Кислородный баланс взрывчатых веществ (часть 1)
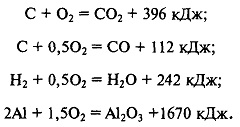
В соответствии с законами химической термодинамики реакция взрывчатого превращения ВВ должна протекать в направлении образования наиболее устойчивых соединений и выделения максимального количества энергии. Таким образом, кислород, входящий в состав ВВ, должен расходоваться в первую очередь на окисление алюминия, затем водорода до Н2О и, наконец, углерода до СО2 (при этом соответственно выделяется 557, 242 и 198 кДж энергии в пересчете на один атом кислорода).
Однако в каждом конкретном случае на ход реакции взрывчатого превращения оказывают влияние многие факторы: качество заряжания, плотность ВВ, температура газообразных продуктов взрыва (ПВ), химический состав пород, влажность рудничного воздуха и др. Поэтому истинную реакцию взрыва составить практически невозможно и при расчете термодинамических параметров принимается упрощенный метод, согласно которому все реакции взрывчатого превращения сводятся к одному из трех видов в зависимости от количества содержащегося в ВВ кислорода: 1) кислорода достаточно (может быть с избытком) для полного окисления горючих компонентов; 2) кислорода достаточно для полного газообразования; 3) кислорода не достаточно для полного газообразования.
Количество кислорода во взрывчатом веществе характеризуется кислородным балансом. Под кислородным балансом (КБ) понимается отношение избытка или недостатка кислорода в ВВ (по сравнению с тем его количеством, которое необходимо для полного окисления горючих компонентов) к молекулярной массе ВВ.
Полное окисление — химическая реакция, в результате которой образуется наивысший оксид горючего компонента (Аl2O3, Н2O, СO2) и, следовательно, выделяется максимальное количество энергии.
- Общие понятия о взрыве и взрывчатых веществах (часть 3)
- Общие понятия о взрыве и взрывчатых веществах (часть 2)
- Общие понятия о взрыве и взрывчатых веществах (часть 1)
- Разрушение горных пород взрывом
- Радиоактивные газы
- Содержание радиоактивных элементов в земной коре
- Радиоактивные свойства минералов и горных пород. Общие сведения
- Магнитные свойства (часть 2)
- Магнитные свойства (часть 1)
- Поляризуемость горных пород. Пьезоэлектрический эффект
- Удельное электрическое сопротивление
- Тепловое расширение, плавкость, полиморфные превращения минералов
- Теплопроводность и температуропроводность пород (часть 2)
- Теплопроводность и температуропроводность пород (часть 1)
- Теплоемкость горных пород (часть 2)
- Теплоемкость горных пород (часть 1)
- Твердость и пластичность. Трещиноватость (часть 2)
- Твердость и пластичность. Трещиноватость (часть 1)
- Дробимость. Метод толчения падающим грузом
- Буримость и взрываемость
- Абразивность
- Горнотехнические свойства. Понятие о крепости горных пород
- Паспорт прочности горных пород
- Прочность пород при растяжении, сдвиге, изгибе (часть 2)
- Прочность пород при растяжении, сдвиге, изгибе (часть 1)
- Прочность пород при сжатии (часть 2)
- Прочность пород при сжатии (часть 1)
- Прочностные свойства горных пород. Общие сведения
- Деформационные свойства при динамическом нагружении
- Определение модуля упругости и коэффициента Пуассона (часть 2)

