Процесс растворения (часть 2)
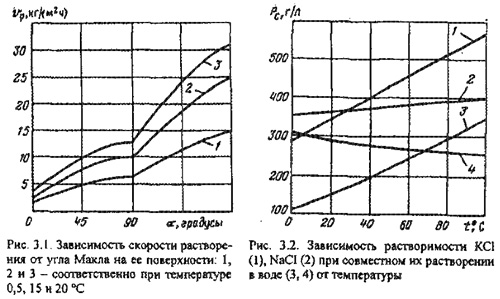
Давление оказывает влияние на растворимость солей при очень высоких его значениях. Так, например, увеличение давления до 25 МПа повышает растворимость хлористого натрия на 2 г/л. Это важно учитывать при подземном растворении во избежание извлечения на поверхность пересыщенных растворов и кристаллизации солей в трубопроводах.
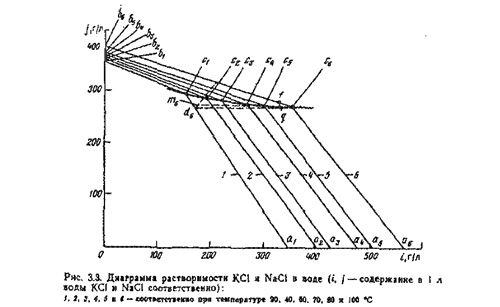
На рис. 3.3 приведена диаграмма растворимости в системе KCI-NaCl-H2О. Точки а1-а6 на оси абсцисс и b1-b6 на оси ординат диаграммы соответствуют содержанию хлористого калия и натрия в граммах в 1 л воды при различной температуре раствора. При постепенном добавлении к указанным растворам хлористого натрия или хлористого калия точки а1-а6 или b1-b6 переместятся по линиям диаграммы соответственно в точки c1-с6. Линии, проведенные из точек а1, а2,..., а6 и из точек b1, b2, b3, ...,b3, пересекутся в точках с1, с2, ..., с6 которые и будут соответствовать растворам, насыщенным одновременно хлористым калием и натрием при соответствующей температуре. Растворы, насыщенные обеими солями, не будут растворять этих солей. На линиях (изотермах) a1c1, a2c2 ..., а6с6 располагаются точки, соответствующие растворам, которые насыщены хлористым калием и не насыщены хлористым натрием, а на изотермах b1c1, b2c2, ..., b6c6 - точки, соответствующие растворам, насыщенным натрием и не насыщенным хлористым калием. На линии с1 с6 (политерма) располагаются точки, соответствующие рассолам, насыщенным обеими солями при температуре от 20 до 100°С. Если раствор, соответствующий точке d6 (раствор насыщения обеими солями при температуре 100°С), охладить до 20°С, то состав его будет изменяться по кривой кристаллизации c6d6, параллельной оси абсцисс, так как соотношение воды и хлористого натрия остается в этом случае неизменным. Раствор, соответствующий точке d6, насыщен хлористым калием, но не насыщен хлористым натрием при температуре 20°С. Поэтому при охлаждении раствора от 100 до 20°С часть хлористого калия выпадает в осадок. Если раствор, соответствующий точке d6 снова нагреть до 100°С, то он растворит недостающую часть хлористого калия. Содержание хлористого натрия в растворе останется неизменным.
- Процесс растворения (часть 1)
- Химия геотехнологических процессов (часть 6)
- Химия геотехнологических процессов (часть 5)
- Химия геотехнологических процессов (часть 4)
- Химия геотехнологических процессов (часть 3)
- Химия геотехнологических процессов (часть 2)
- Химия геотехнологических процессов (часть 1)
- Физико-химические основы геотехнологических процессов
- Геолого-гидрологические работы на предприятиях, работающих ФХМГ (часть 4)
- Геолого-гидрологические работы на предприятиях, работающих ФХМГ (часть 3)
- Геолого-гидрологические работы на предприятиях, работающих ФХМГ (часть 2)
- Геолого-гидрологические работы на предприятиях, работающих ФХМГ (часть 1)
- Основные технологические зависимости
- Оптимизации параметров геотехнологического производства (часть 2)
- Оптимизации параметров геотехнологического производства (часть 1)
- Методика расчета основных параметров добычи
- Анализ экономики вскрытий месторождения (часть 2)
- Анализ экономики вскрытий месторождения (часть 1)
- Расчет себестоимости полезного ископаемого
- Производительность труда и себестоимость добычи
- Структура капитальных вложений
- Гидрогеологические исследования (часть 2)
- Методика выбора метода разработки (часть 2)
- Гидрогеологические исследования (часть 1)
- Исследование месторождения при подготовке его к отработке ФХМГ (часть 3)
- Исследование месторождения при подготовке его к отработке ФХМГ (часть 2)
- Исследование месторождения при подготовке его к отработке ФХМГ (часть 1)
- Методика выбора метода разработки (часть 1)
- Требования методов ФХГ к физико-геологической обстановке
- Физико-геологические факторы - ФХМГ (часть 2)

