Процесс выщелачивания (часть 2)
Совокупность этих двух процессов представляет собой конвективную диффузию вещества в жидкости. Полный поток вещества при конвективной диффузии через 1 см2 поверхности будет
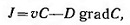
где D — коэффициент диффузии; С — концентрация смеси; v — скорость движения смеси.
Для решения общего уравнения конвективной диффузии в качестве граничных условий обычно принимается концентрация раствора или ее производная на границе общей диффузии. Это уравнение применимо как для условий движения свободной жидкости, так и для условий движения жидкости в пористой среде. Разница лишь в том, что во втором случае необходимо использовать эффективный коэффициент диффузии внутри массы пористого материала, который определяется средним диаметром пор, их числом на единицу площади и коэффициентом извилистости.
Следовательно, установление кинетических закономерностей процесса извлечения вещества в пористой среде связано с решением дифференциальных уравнений молекулярной и конвективной диффузии с учетом влияния формы, размеров и полидисперсности частиц, длины слоя, концентрации растворителя, гидродинамики движения жидкости.
В приложении к большинству диффузионных процессов извлечения из пористых сред эта задача чрезвычайно сложна. До настоящего времени нет общепризнанной законченной теории извлечения компонентов из слоя пористых тел и во многих случаях невозможно научно обосновать выбор селективного растворителя и условий растворения. Теоретические представления в этой области получают все большее развитие. В этом большая заслуга Н. Н. Веригина, Г. А. Аксельруда, М. А. Альтшулера, Е. М. Семенишина и других исследователей.
Кинетика процессов растворения описывается уравнением
Скорость межфазовых процессов зависит от природы твердого тела, а в конечном итоге — от энергии активации, рассчитываемой по уравнению Аррениуса.
Способность минералов растворяться зависит от температуры, химической устойчивости, обусловленной прочностью кристаллической решетки, величиной и структурой поверхности реагирования минерала с растворителем.
Кроме диффузионных и термодинамических параметров, существенным фактором, определяющим кинетику процесса химического растворения, является гравитационная конвекция.
Методы химического извлечения минералов, основанные на выщелачивании, предусматривают, как правило, селективное извлечение полезного компонента, которое базируется на различной химической устойчивости отдельных минералов. Теоретической предпосылкой оценки химической селекции минералов может служить соотношение свободной энергии или теплоты их образования.
Химическая устойчивость минералов может быть сопоставлена на основании непосредственного расчета энергии кристаллической решетки. Для этого пользуются формулой А. Ф. Капустинского.
Термодинамические величины не всегда позволяют правильно оценить химическую устойчивость минералов вследствие близости в энергетическом отношении некоторых различных структур. В таких случаях относительная химическая устойчивость минералов оценивается на основании сопоставления кинетики взаимодействия минералов с растворителями.
- Процесс выщелачивания (часть 1)
- Процесс растворения (часть 2)
- Процесс растворения (часть 1)
- Химия геотехнологических процессов (часть 2)
- Химия геотехнологических процессов (часть 1)
- Физико-химические основы геотехнологических процессов
- Геолого-гидрогеологические работы (часть 4)
- Геолого-гидрогеологические работы (часть 3)
- Геолого-гидрогеологические работы (часть 2)
- Геолого-гидрогеологические работы (часть 1)
- Методика исследований месторождения (часть 5)
- Методика исследований месторождения (часть 4)
- Методика исследований месторождения (часть 3)
- Методика исследований месторождения (часть 2)
- Методика исследований месторождения (часть 1)
- Требования геотехнологических методов
- Физико-геологические факторы и эффективность обработки (часть 2)
- Физико-геологические факторы и эффективность обработки (часть 1)
- Горная среда, горная порода, полезные ископаемые (часть 5)
- Горная среда, горная порода, полезные ископаемые (часть 4)
- Горная среда, горная порода, полезные ископаемые (часть 3)
- Горная среда, горная порода, полезные ископаемые (часть 2)
- Горная среда, горная порода, полезные ископаемые (часть 1)
- Физико-геологические основы геотехнологии
- Основные направления развития геотехнологии (часть 2)
- Основные направления развития геотехнологии (часть 1)
- Основные понятия и определения (часть 3)
- Основные понятия и определения (часть 2)
- Основные понятия и определения (часть 1)
- Особенности геотехнологических методов и их классификация


